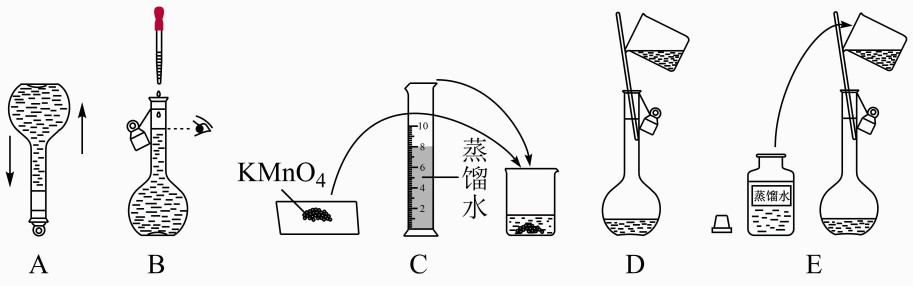
1.
Ⅰ.实验室欲配制的
溶液
:
(1)配制溶液时必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管和。
(2)若用 晶体来配制该溶液,应称量晶体的质量为g。
晶体来配制该溶液,应称量晶体的质量为g。
(3)容量瓶使用前必须进行的操作是。
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是(填序号)。
①没有洗涤烧杯和玻璃棒
②容量瓶未干燥,且瓶内有少量蒸馏水
③用托盘天平称量晶体时,药品和砝码放反了
④定容时俯视刻度线
⑤定容后塞上瓶塞反复摇匀,静置后,发现液面低于刻度线,再加水至刻度线
Ⅱ.某化学实验室需要硫酸溶液
。根据溶液的配制情况回答下列问题:
(5)现用质量分数为98%、密度为 的浓硫酸来配制所需的稀硫酸。计算所需浓硫酸的体积为
的浓硫酸来配制所需的稀硫酸。计算所需浓硫酸的体积为 (保留1位小数),现有①
(保留1位小数),现有① 、②
、② 、③
、③ 、④
、④ 四种规格的量筒,你选用的量筒是(填序号)。
四种规格的量筒,你选用的量筒是(填序号)。
(6)配制时,一般可分为几个步骤:①量取 ②计算 ③摇匀 ④稀释 ⑤冷却 ⑥洗涤 ⑦定容 ⑧转移,其正确的操作顺序为②→①→④→___→____→____→___→③(填序号) 。
【考点】
常用仪器及其使用;
配制一定物质的量浓度的溶液;
基础巩固
能力提升
变式训练
拓展培优




 泥三角
泥三角



 C.量筒
C.量筒