1.
实验室需要90mL1.0mol•L-1稀硫酸,现用质量分数为98%、密度为1.84g/mL的浓硫酸配制,根据实验事实需要配制情况回答下列问题。
(1)
需量取浓硫酸的体积为mL。
(2)
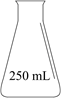
在如图所示仪器中,配制上述溶液肯定不需要的是(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是。
(3)
在容量瓶的使用方法中,下列操作不正确的是___________。
A.
使用容量瓶前检验是否漏水
B.
容量瓶用水洗净后,再用待配溶液洗涤
C.
配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.
定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(4)
配制过程中,下列情况会使配制结果偏高的是(填序号),偏低的是 ,不影响的是。
(5)
若用0.01000mol·L-1K2Cr2O7(酸性)溶液滴定20.00mL未知浓度的含Fe2+的溶液,恰好完全反应时消10.00mLK2Cr2O7溶液,则待测液中Fe2+的浓度是 mol/L。
A.![]() B.
B. C.
C.![]() D.
D. E.
E.
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
【考点】
配制一定物质的量浓度的溶液;
中和滴定;
能力提升
真题演练