1.
TiO2-aNb、Cu(In1-xGaxSe2)是常见的光学活性物质。请回答下列问题:
(1)
基态Ti原子的电子所占据的最高能层符号为,N、O、Cu的电负性由大到小的顺序是。
(2)
利用TiO2纳米管的光电实验可制备TNT(2,4,6—三硝基甲苯),其结构如图,N原子的杂化类型为。TNT常温下是固体,而甲苯是液体,原因是。
(3)
GaCl3·xNH3(x=3,4,5,6)是一系列化合物,向含1molGaCl3·xNH3的溶液中加入足量AgNO3溶液,有难溶于硝酸的白色沉淀生成;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1:2。
(4)
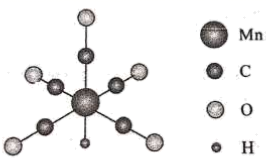
TiO2通过氮掺杂反应生成TiO2-aNb , 表示如图。

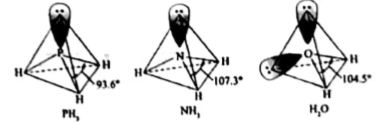
①NH3的VSEPR模型为。
②GaCl3·xNH3含有的化学键类型有(填序号)。
A.极性共价键 B.离子键 C.配位键 D.金属键 E.氢键
③能准确表示GaCl3·xNH3结构的化学式为。

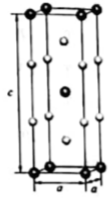
①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为g/cm3。
②图乙TiO2-aNb晶体中a=。
【考点】
配合物的成键情况;
晶胞的计算;
能力提升
真题演练