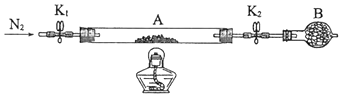
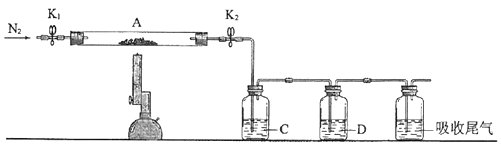
1.
FeOOH是一种不溶于水的黄色固体,在高档涂料、油墨等领域有着广泛的应用。某工厂以 废料(含少量
废料(含少量 、
、 等)为原料制备FeOOH以及回收Al,其工艺流程如图所示:
等)为原料制备FeOOH以及回收Al,其工艺流程如图所示:

已知:
①溶于水,难溶于乙醇;
②下表是25℃不同离子生成氢氧化物沉淀的对应pH:
离子 | 开始沉淀的pH | 完全沉淀的pH |
7.6 | 9.6 | |
2.2 | 3.7 | |
3.4 | 4.7 |
回答下列问题:
(1)
为提高“酸浸”的速率,可采取的措施是(任填一种)。
(2)
“酸浸”主要发生的离子方程式有: 、;“滤渣”的主要成分为(填名称)。
(3)
“还原”的目的是将
、;“滤渣”的主要成分为(填名称)。
(3)
“还原”的目的是将 还原为
还原为 , “试剂X”可选择___________(填标号)。
A.
铁粉
B.
氯气
C.
, “试剂X”可选择___________(填标号)。
A.
铁粉
B.
氯气
C.
 D.
铜粉
(4)
请简述检验“还原”后溶液中有无
D.
铜粉
(4)
请简述检验“还原”后溶液中有无 的方法(写出操作过程、现象及结论):。
(5)
“沉铝”时,溶液的pH范围应调为。
(6)
向“滤液1”中加入乙醇的作用是。
(7)
由
的方法(写出操作过程、现象及结论):。
(5)
“沉铝”时,溶液的pH范围应调为。
(6)
向“滤液1”中加入乙醇的作用是。
(7)
由 转化为FeOOH的离子方程式为,“滤液2”的溶质主要为(填化学式)。
转化为FeOOH的离子方程式为,“滤液2”的溶质主要为(填化学式)。
【考点】
铁盐和亚铁盐的相互转变;
二价铁离子和三价铁离子的检验;
能力提升
真题演练