1.
甲醛有毒,能使人体内蛋白质失去活性,损害人体健康。
(1)
蛋白质中主要含有 、
、 、
、 、
、 四种元素。
(2)
酸性高锰酸钾溶液、新制氧化银等氧化剂能去除甲醛。
(3)
甲醛使蛋白质失活的第一步反应如下,二者遵循“正找负、负找正”的规律发生加成反应。
四种元素。
(2)
酸性高锰酸钾溶液、新制氧化银等氧化剂能去除甲醛。
(3)
甲醛使蛋白质失活的第一步反应如下,二者遵循“正找负、负找正”的规律发生加成反应。
①下列关于C、H、O、N的说法中,正确的是(填序号)。
a.的电子云呈球形 b.
、
、
、
中,
的原子半径最大
c.、
、
、
均位于
区 d.基态O中含有8种不同运动状态的电子
②第一电离能 , 原因是。
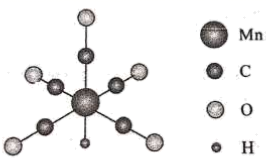
①基态Mn原子的价电子排布式为。
②已知基态Ag原子的简化电子排布式为 , 银元素在周期表中的位置是。
已知:部分元素电负性:C2.5、H2.1、O3.5、N3.0

①结合电负性解释与N相连的H带部分正电荷的原因:。
②补全第二步反应(断键位置已用虚线标出,反应类型为取代反应)。

【考点】
原子核外电子排布;
元素电离能、电负性的含义及应用;
能力提升
真题演练