1.
铜是人类广泛使用的一种金属,含铜物质在生产、生活中有着广泛应用。回答下列问题:
(1)
铜锰氧化物(CuMn2O4)能在常温下催化氧化CO。
(2)
已知硫酸铜稀溶液呈天蓝色,其中铜离子以 形式存在,判断硫酸铜稀溶液中不存在的作用力有(填标号)。
(3)
形式存在,判断硫酸铜稀溶液中不存在的作用力有(填标号)。
(3)
 可形成
可形成 , 其中X代表
, 其中X代表 , 则
, 则 中配位原子为(填元素符号),配位数为。1 mol
中配位原子为(填元素符号),配位数为。1 mol  +微粒中VSEPR模型为四面体的非金属原子共有mol。
+微粒中VSEPR模型为四面体的非金属原子共有mol。 中
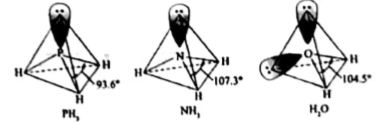
中 键角(填“>”“<”或“=”)
键角(填“>”“<”或“=”) 分子中
分子中 键角,原因是。
(4)
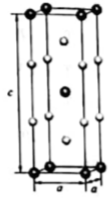
CuInS2(相对分子质量为Mr)是生物医药、太阳能电池等领域的理想荧光材料,其晶胞结构如图所示,则CuInS2晶体的密度为
键角,原因是。
(4)
CuInS2(相对分子质量为Mr)是生物医药、太阳能电池等领域的理想荧光材料,其晶胞结构如图所示,则CuInS2晶体的密度为 (列出计算式即可,阿伏加德罗常数用
(列出计算式即可,阿伏加德罗常数用 表示)。
表示)。
①基态Cu原子价电子排布式为。
②与CO互为等电子体的分子为(任写一种),标准状况下V L CO分子中π键的物质的量为mol。
③锰在元素周期表中位于(填“s”“p”“d”或“ds”)区。
A.配位键 B.金属键 C.离子键 D.氢键 E.范德华力

【考点】
判断简单分子或离子的构型;
配合物的成键情况;
晶胞的计算;
原子轨道杂化方式及杂化类型判断;
能力提升
真题演练