1.
回答下列问题。
(Ⅰ). 某化学实验小组为探究和比较和氯水的漂白性,设计了如图的实验装置。

回答下列问题:
(1)装置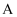 中盛装浓硫酸的仪器名称是 ,实验室用装置
中盛装浓硫酸的仪器名称是 ,实验室用装置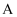 制备
制备 , 发生反应的化学方程式为 。
, 发生反应的化学方程式为 。
(2)实验室用装置 制备
制备 , 其反应的化学方程式为 ,若有
, 其反应的化学方程式为 ,若有 参加反应,则转移的电子总数为 。
参加反应,则转移的电子总数为 。
(3)反应开始一段时间后,观察到 、
、 两个试管中的品红溶液都褪色,停止通气后,再给
两个试管中的品红溶液都褪色,停止通气后,再给 、
、 两个试管分别加热;两个试管中的现象分别为:
两个试管分别加热;两个试管中的现象分别为: : ,
: , 。
。
(4)小组中甲同学认为 和氯水都有漂白性,若二者混合使用,漂白性会更强。为验证甲同学的推断,在同温同压下,他们同时将
和氯水都有漂白性,若二者混合使用,漂白性会更强。为验证甲同学的推断,在同温同压下,他们同时将 和
和 等体积通入到品红溶液中,结果发现品红溶液几乎不褪色,出现上述现象的原因是 。
等体积通入到品红溶液中,结果发现品红溶液几乎不褪色,出现上述现象的原因是 。 用化学方程式表示
用化学方程式表示
(Ⅱ).某同学做如下实验,以检验反应中的能量变化。

(5)在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是热反应;(b)中温度降低,由此可以判断(b)中反应是热反应。
(6)写出铝与盐酸反应的离子方程式:。
(7)根据能量守恒定律,(b)中反应物的总能量应该生成物的总能量(填“低于”或“高于”)。
【考点】
氯气的实验室制法;
能力提升
变式训练
拓展培优
真题演练











