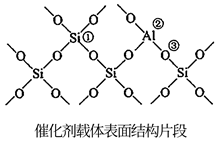
1.
为尽快实现“碳达峰”“碳中和”,碳化学研究已成为当前科学研究的热点。由 合成淀粉的部分流程如图所示:
合成淀粉的部分流程如图所示:

图中涉及的部分热化学方程式如下:
①
②
③
④
回答下列问题:
(1)
反应①中,反应物的总能量(填“大于”、“小于”或“等于”,下同)生成物的总能量,反应④中,反应物的总键能生成物的总键能。
(2)
反应①中使用催化剂的作用有(填标号);将3mol 和1mol
和1mol 通过催化剂发生反应①,经过2次循环后测得
通过催化剂发生反应①,经过2次循环后测得 的转化率为36%,则经过4次循环后
的转化率为36%,则经过4次循环后 的转化率为。
(3)
已知
的转化率为。
(3)
已知 的燃烧热(
的燃烧热( )为
)为 , 则
, 则 的燃烧热(
的燃烧热( )为。
(4)
)为。
(4)
 合成淀粉过程中,当有1kg
合成淀粉过程中,当有1kg 转化为
转化为 时,理论上反应体系共需向外界(填“吸收”或“放出”)的热量为kJ。(所有能量均充分利用,且不考虑能量的损耗)
(5)
几个有关CO的热化学方程式为
时,理论上反应体系共需向外界(填“吸收”或“放出”)的热量为kJ。(所有能量均充分利用,且不考虑能量的损耗)
(5)
几个有关CO的热化学方程式为
 ;
;
a.有效降低了反应活化能
b.提高了的平衡转化率
c.加快了反应①的反应速率
;
;
则
(用含
、
、
的代数式表示)。
【考点】
反应热和焓变;
盖斯定律及其应用;
能力提升
真题演练






 (g) ∆H1<0
(g) ∆H1<0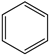 (g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4
(g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4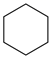 (g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5
(g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5