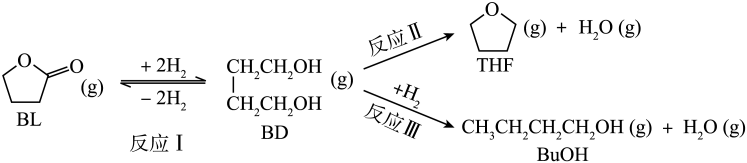
1.
能源短缺是全球面临的问题,用 来生产燃料甲醇可缓解能源危机。反应原理为
来生产燃料甲醇可缓解能源危机。反应原理为 。回答下列问题:
。回答下列问题:
(1)
已知某些化学键的键能数据如下表所示。则该反应的
 。
。
(2)
向恒容恒温密闭容器中充入一定量的 和
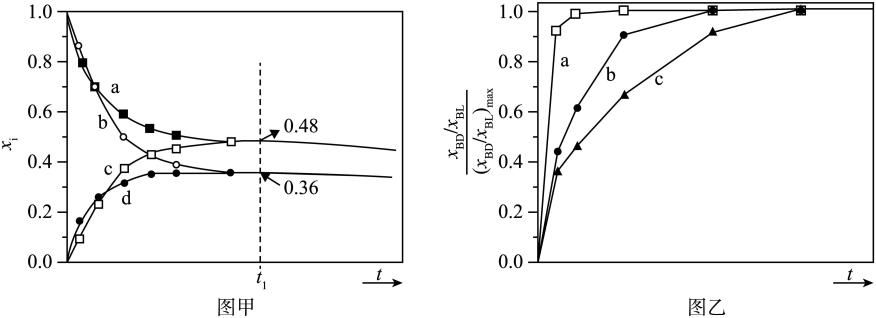
和 发生上述反应,图中过程Ⅰ、Ⅱ是在两种不同催化剂作用下建立平衡的过程中
发生上述反应,图中过程Ⅰ、Ⅱ是在两种不同催化剂作用下建立平衡的过程中 的转化率[
的转化率[ ]随时间(t)的变化曲线。
(3)
在起始物
]随时间(t)的变化曲线。
(3)
在起始物 时,上述反应在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,上述反应在不同条件下达到平衡,设体系中甲醇的物质的量分数为 , 在T=250℃下的
, 在T=250℃下的 ~p、在
~p、在 下的
下的 ~T如图所示。
~T如图所示。
化学键 | C-H | H-H | C-O | C=O | H-O |
键能/( | 413.4 | 436.0 | 351.0 | 745.0 | 462.8 |

①m点:(填“>”或“<”)
。
②活化能:过程Ⅱ(填“>”或“<”)过程Ⅰ。
③过程Ⅰ,时刻改变的反应条件可能是(任写一种)。

①用各物质的平衡分压表示总反应的平衡常数,表达式
②图中对应等压过程的曲线是。
③当时,
的平衡转化率
(保留一位小数)。
【考点】
反应热和焓变;
能力提升
真题演练