1.
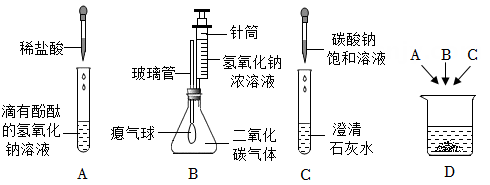
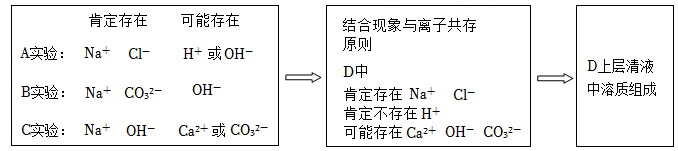
小科利用如图所示装置(气密性良好)探究二氧化硫、亚硫酸钠(Na2SO3)等物质的性质,实验方案如下:

【查阅资料】
①二氧化硫的化学性质类似于二氧化碳:②二氧化硫易溶于水;③亚硫酸钙(CaSO3)白色、难溶于水。
【实验步骤】
Ⅰ.先关闭止水夹,将注射器1中足量的氢氧化钠溶液压入充满二氧化硫的三颈烧瓶中;
Ⅱ.充分反应后,再打开止水夹,并观察、记录实验现象;
Ⅲ.对实验进行分析,并深入探究“三颈烧瓶内液体的溶质可能是什么”。
【交流评价】
(1)
步骤Ⅱ的烧瓶中观察到的现象是。
(2)
不能由步骤Ⅱ的现象得出“SO2与 NaOH 发生了反应”的结论,其原因是。
(3)
步骤Ⅲ中,猜想有:①溶质是氢氧化钠;②溶质是氢氧化钠和氢氧化钙:③溶质是氢氧化钠和亚硫酸钠。为验证猜想②,小科的方案是:在注射器2中装入适量的Na2CO3溶液,压入三颈烧瓶中,并观察实验现象。请对小科的方案进行评价。
【考点】
实验方案设计与评价;
碱的化学性质;
能力提升
真题演练