1.
下列实验方案能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 鉴别稀盐酸和稀硫酸溶液 | 加入硝酸银溶液,观察现象 |
B | 检验氢氧化钠溶液变质程度 | 先加过量的氯化钡,过滤后向滤液中加入酚酞 |
C | 除去二氧化碳中混有的氯化氢 | 将气体通过足量的氢氧化钠溶液 |
D | 除去MnO2中混有的KCl | 加水溶解、蒸发结晶 |
A.
A
B.
B
C.
C
D.
D
【考点】
物质除杂或净化;
物质的鉴别、推断;
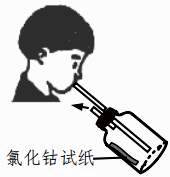
 检验甲烷燃烧有CO2生成
检验甲烷燃烧有CO2生成 将带有残留夜的滴管倒持
将带有残留夜的滴管倒持 吹灭酒精灯
吹灭酒精灯

