1.
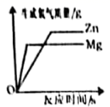
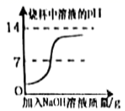
某品牌炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学为测定该炉具清洁剂中氢氧化钠的质量分数,做了如下探究,取10.0g炉具清洁剂样品于烧杯中,加水稀释,再逐滴加入溶质质量分数为0.73%的稀盐酸(密度是1.0g/mL),并用玻璃棒不断搅拌(如图1所示)。同时利用pH传感器测定溶液的pH,反应过程中溶液的pH随加入稀盐酸的体积变化关系如图2所示。(已知:该清洁剂中其他成分不与水、稀盐酸发生反应)

【考点】
中和反应及其应用;
根据化学反应方程式的计算;
基础巩固
能力提升
变式训练
拓展培优
真题演练