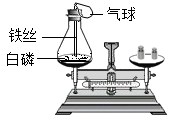
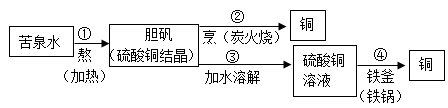
1.
某化学反应的反应物和生成物的微观示意图及反应前后的质量如表所示。
|
物质 |
甲 |
乙 |
丙 |
丁 |
|
|
微观示意图 |
|
|
|
|
|
|
反应前质量/g |
32 |
200 |
1 |
0 |
|
|
反应后质量/g |
0 |
x |
y |
z |
下列有关该反应的说法正确的是( )
A.
甲物质由碳原子和氢原子直接构成
B.
该反应属于置换反应
C.
参加反应的反应物分子个数比为1:1
D.
x+y+z=233
【考点】
质量守恒定律及其应用;
能力提升
变式训练
拓展培优
真题演练





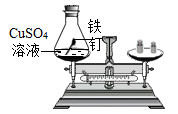

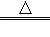 Te↓+3H2SO4 , 则X为 (填化学式).
Te↓+3H2SO4 , 则X为 (填化学式).