1.
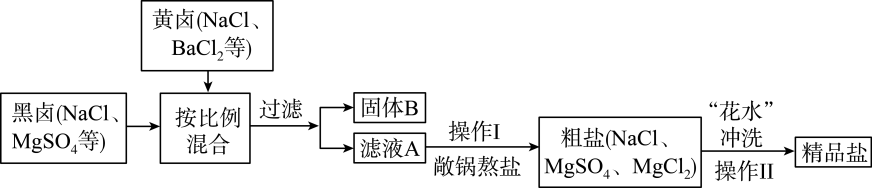
古籍中有关“敞锅熬盐”记载主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,析出粗盐;③用“花水”冲洗粗盐得精品盐。其流程如图所示:
(1)
操作1敞锅熬盐的过程称为。
(2)
黄卤和黑卤混合后发生反应的化学方程式为。
(3)
根据粗盐的成分可知,步骤①加入的(“黄卤”或“黑卤”)过量,操作Ⅱ用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl,则“花水”应当是。
(4)
“精品盐”在生成生活中有着广泛的用途,医疗上用来配制。
【考点】
粗盐提纯;
物质除杂或净化的探究;
能力提升
真题演练


