1.
 和
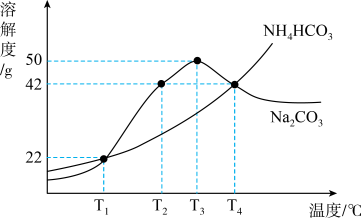
和 的溶解度曲线如图所示,下列叙述正确的是( )
的溶解度曲线如图所示,下列叙述正确的是( )

A.
 和
和 都属于易溶物质
B.
都属于易溶物质
B.
 时,
时, 饱和溶液中溶解了
饱和溶液中溶解了 C.
C.
 时,
时, 溶液的溶质质量分数一定大于
溶液的溶质质量分数一定大于 溶液的溶质质量分数
D.
当
溶液的溶质质量分数
D.
当 中混有少量
中混有少量 杂质时,可采取冷却
杂质时,可采取冷却 热饱和溶液的方法提纯
热饱和溶液的方法提纯
【考点】
固体溶解度曲线及其作用;
能力提升
变式训练
拓展培优
真题演练