1.
科学探究是认识和解决化学问题的重要实践活动。
近年来,自热食品种类繁多。只需将撕去塑料膜的发热包放入凉水中,就能享用美食,很受年轻人的追捧。实验小组同学买来一份自热食品进行以下探究。
【资料】Ⅰ、发热包中物质的主要成分是生石灰、碳酸钠、铝粒。
Ⅱ、铝能和NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,偏铝酸钠溶于水。
(1)
探究一:发热包的发热原理。
(2)
在使用发热包过程中,禁止明火的理由是。
(3)
探究二:反应后混合物中部分成分的探究。
(4)
根据现象①得出:滤液A中一定不含的物质是。根据现象②③分析得出:固体B中一定含有的物质是。综合分析得出:现象③中产生的气体,其成分的组成可能为。
(5)
通过以上探究,同学们进行反思总结,你认为其中正确的是____。
A.
能与水混合放出热量的物质均可做发热包的发热材料
B.
发热包应密封防潮保存
C.
禁止用湿手接触发热包
D.
使用过程中应保持通风
小组同学取出发热包,撕去塑料膜,放入适量凉水中,可观察到的现象是,固体迅速膨胀,同时还可观察到发热包内固体变硬结块,其可能的原因是(用化学方程式表示)。
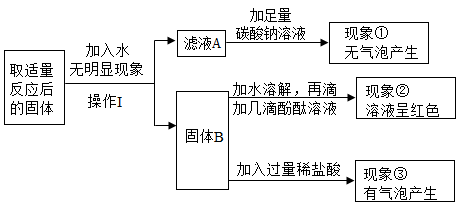
根据以上操作和实验现象回答下列问题。
操作Ⅰ的名称是。
【考点】
食品干燥剂、保鲜剂和真空包装的成分探究;
实验探究物质的组成成分以及含量;
化学实验方案设计与评价;
能力提升



