1.
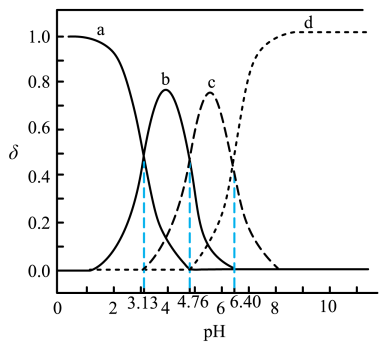
常温时,某浓度的二元弱酸 溶液在不同pH下测得pc(M)变化如图所示[已知:
溶液在不同pH下测得pc(M)变化如图所示[已知: , M代指
, M代指 或
或 或
或 ],下列说法正确的是( )
],下列说法正确的是( )

A.
NaHB溶液中, B.
X点的pH为4.06
C.
B.
X点的pH为4.06
C.
 时,
时, D.
D.
 的值为
的值为
【考点】
pH的简单计算;
离子浓度大小的比较;
能力提升
变式训练
拓展培优
真题演练