1.
丙烯是一种重要的化工原料,可以在催化剂作用下,由丙烷直接脱氢或氧化脱氢制备。
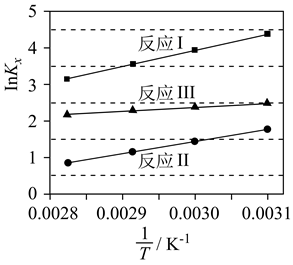
反应Ⅰ(直接脱氢):C3H8(g)=C3H6(g)+H2(g)△H1=+125kJ·mol-1
反应Ⅱ(氧化脱氢):C3H8(g)+ O2(g)=C3H6(g)+H2O(g)△H2=-118kJ·mol-1
(1)
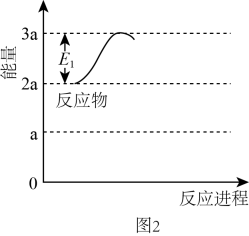
已知键能:E(C—H)=416kJ·mol-1 , E(H—H)=436kJ·mol-1 , 由此计算生成1mol碳碳π键放出的能量为kJ。
(2)
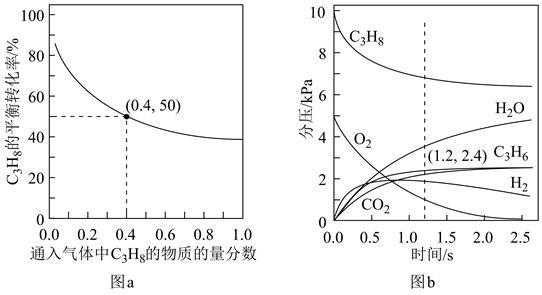
对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入C3H8和N2的混合气体(N2不参与反应),从平衡移动的角度判断,达到平衡后“通入N2”的作用是。在温度为T1时,C3H8的平衡转化率与通入气体中C3H8的物质的量分数的关系如图a所示,计算T1时反应Ⅰ的平衡常数Kp=kPa(以分压表示,分压=总压×物质的量分数,保留一位小数)。
(3)
在温度为T2时,通入气体分压比为p(C3H8):p(O2):p(N2)=10:5:85的混合气体,各组分气体的分压随时间的变化关系如图b所示。0~1.2s生成C3H6的平均速率为kPa·s-1;;在反应一段时间后,C3H8和O2的消耗速率比小于2∶1的原因为。
(4)
恒温刚性密闭容器中通入气体分压比为p(C3H8):p(O2):p(N2)=2:13:85的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):
反应Ⅱ:2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) k
反应Ⅲ:2C3H6(g)+9O2(g)=6CO2(g)+6H2O(g) k′
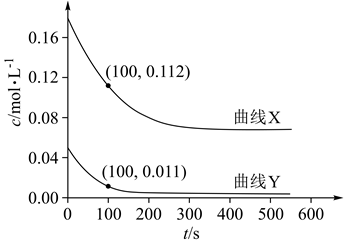
实验测得丙烯的净生成速率方程为v(C3H6)=kp(C3H8)-k′p(C3H6),可推测丙烯的浓度随时间的变化趋势为,其理由是。
【考点】
化学反应速率与化学平衡的综合应用;
能力提升
真题演练







 △H1
△H1 △H2
△H2