1.
已知:  。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如下探究。
。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如下探究。
(1)
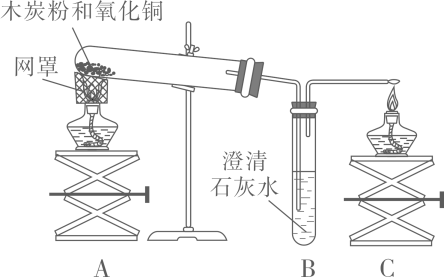
I.设计如实验装置,开展氢气还原氧化铜实验并检验固体产物。
(2)
氧化钙的作用是。
(3)
取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到,证明固体产物有Cu2O。
(4)
II.探究反应生成Cu2O的变化情况。
(5)
为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是。
(6)
III.探究反应生成Cu2O的原因。
(7)
若要确认“假设2”是否合理,在探究II的基础上,还需进行的实验是。

制取氢气的化学方程式为。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图。

由图可知,在氢气还原氧化铜反应过程中,Cu2O质量的变化趋势是。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1.经历 、
两个反应,且在同一条件下两个反应同时进行。
假设2.经历 、
、
三个反应。
结合探究II结果计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是。
【考点】
碳、一氧化碳、氢气还原氧化铜实验;
实验探究物质的性质或变化规律;
能力提升
真题演练