1.
根据题意解答
(1)
肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.
(2)
肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如图所示,回答下列问题:
(3)
LiCoO2可用作一种锂离子电池的正极材料.该锂离子电池充电过程中,负极发生的反应为6C+xLi++xe﹣═LixC6 , 正极发生LiCoO2与Li1﹣xCoO2之间的转化,写出放电时电池总反应方程式.
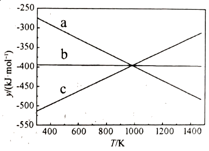
已知:①N2(g)+2O2(g)=N2O4 (g)△H1=﹣195kJ•mol﹣1
②N2H4 (1)+O2(g)=N2(g)+2H2O(g)△H2=﹣534.2kJ•mol﹣1
写出肼和N2O4 反应的热化学方程式;

①该燃料电池的负极发生的反应式为.
②电池工作时,OH﹣移向极(“a”或“b”)
③当电池放电转移5mol电子时,至少消耗燃料肼 g.
【考点】
热化学方程式;
能力提升
真题演练
 B.
B. C.
C.