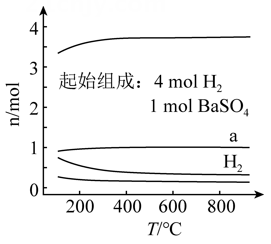
1.
高粱酿酒过程中的部分流程按顺序排列如下,其中能说明高粱转化过程中放出热量的是( )

A.
A
B.
B
C.
C
D.
D
【考点】
吸热反应和放热反应;
基础巩固
能力提升
变式训练
拓展培优
真题演练
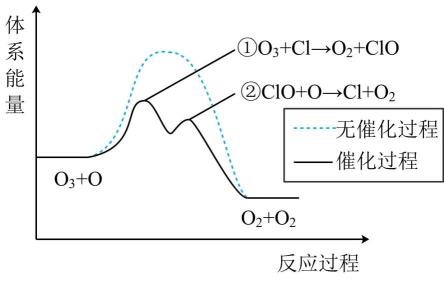








 B.
B.  C.
C. D.
D.