1.
环己烯是重要的化工原料。其实验室制备流程如下:
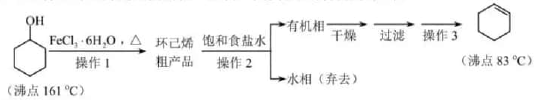
回答下列问题:
(1)
Ⅰ.环己烯的制备与提纯
(2)
操作1的装置如图所示(加热和夹持装置已略去)。
(3)
操作2用到的玻璃仪器是。
(4)
将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,,弃去前馏分,收集83℃的馏分。
(5)
Ⅱ.环己烯含量的测定
(6)
下列情况会导致测定结果偏低的是(填序号)。
原料环己醇中若含苯酚杂质,检验试剂为,现象为。

①烧瓶A中进行的可逆反应化学方程式为,浓硫酸也可作该反应的催化剂,选择 而不用浓硫酸的原因为(填序号)。
a.浓硫酸易使原料碳化并产生
b. 污染小、可循环使用,符合绿色化学理念
c.同等条件下,用 比浓硫酸的平衡转化率高
②仪器B的作用为。
在一定条件下,向 环己烯样品中加入定量制得的
,与环己烯充分反应后,剩余的
与足量
作用生成
,用
的
标准溶液滴定,终点时消耗
标准溶液
(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
① ![]()
②
③
滴定所用指示剂为。样品中环己烯的质量分数为(用字母表示)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c. 标准溶液部分被氧化
【考点】
氧化还原反应;
浓硫酸的性质;
有机物的合成;
烯烃;
加成反应;
能力提升

