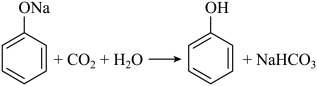
1.
下列离子方程式正确的是( )
A.
向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
B.
二氧化锰和浓盐酸反应:MnO2+4H++2Clˉ Mn2++Cl2↑+2H2O
C.
Al与NaOH溶液反应:2Al+2OH-+6H2O=2Al(OH)3↓+3H2↑
D.
金属钠投入到硫酸铜溶液中:2Na+Cu2+=2Na++Cu
Mn2++Cl2↑+2H2O
C.
Al与NaOH溶液反应:2Al+2OH-+6H2O=2Al(OH)3↓+3H2↑
D.
金属钠投入到硫酸铜溶液中:2Na+Cu2+=2Na++Cu
【考点】
离子方程式的书写;
基础巩固
能力提升
变式训练
拓展培优
真题演练