1.
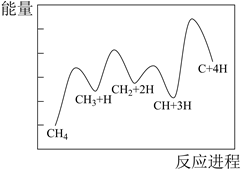
异丙醇 可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯
可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯 的工业化技术已引起人们的关注,其主要反应如下:
的工业化技术已引起人们的关注,其主要反应如下:
Ⅰ.
Ⅱ.
回答下列问题:
(1)
已知 , 则
, 则 燃烧生成
燃烧生成 和
和 的热化学方程式为。
(2)
在
的热化学方程式为。
(2)
在 下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
(3)
在恒温刚性密闭容器中,反应Ⅰ、Ⅱ均达到平衡的判据是(填标号)。
(4)
在一定条件下,若反应Ⅰ、Ⅱ的转化率分别为98%和40%,则丙烯的产率为。
(5)
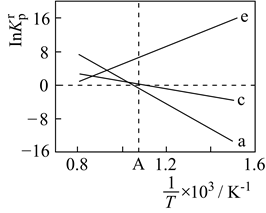
下图为反应Ⅰ、Ⅱ达到平衡时 与温度的关系曲线。
与温度的关系曲线。
反应时间 | 0 | 4 | 8 | 12 | t | 20 |
| 0 | 2440 | 3200 | 3600 | 4000 | 4100 |
①内,
;
②t16(填“>”“<”或“=”)。
a.的分压不变 b.混合气体密度不变
c. d.

(已知:对于可逆反应 , 任意时刻
, 式中
)表示物质×的分压)
①在恒压平衡体系中充入少量水蒸气时,反应Ⅰ的的状态最有可能对应图中的点(填“甲”“乙”或“丙”),判断依据是。
②时,在密闭容器中加入一定量的
, 体系达到平衡后,测得
的分压为
, 则水蒸气的分压为
(用含x的代数式表示)。
【考点】
盖斯定律及其应用;
化学反应速率与化学平衡的综合应用;
能力提升
真题演练