1.
资料显示:久置于潮湿环境中的漂白粉受热生成O2和少量Cl2;干燥的漂白粉加热后发生反应Ca(ClO)2  CaCl2 + O2↑。
CaCl2 + O2↑。
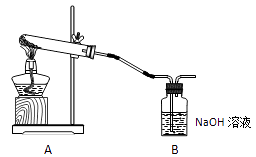
学生甲利用下图装置进行实验:加热A中试管内装有的潮湿漂白粉样品时,观察到B中有大量气泡产生。
(1)
B中发生反应的离子方程式为。
(2)
请写出实验室检验氯气的方法:。
(3)
称量所用仪器名称为;实验到达恒重的判断依据是。
(4)
该漂白粉样品中次氯酸钙的百分含量为(用W1、W2、W3表示);若所用坩埚内壁沾有受热易分解的物质,则该实验测得的结果。(选填“偏大”、“偏小”或“无影响”)
学生乙设计实验测定某干燥漂白粉样品中次氯酸钙的百分含量。实验步骤如下:
①称量坩埚的质量,为W1g。
②坩埚中加入样品后再称,质量为W2g。
③重复进行加热、冷却、称量,直到恒重,质量为W3g。
【考点】
氯气的化学性质;
能力提升
真题演练





 MnCl2+2H2O+Cl2↑,应选用图A、E装置中的 (填序号)制Cl2 , 反应中浓盐酸所表现出的性质是
MnCl2+2H2O+Cl2↑,应选用图A、E装置中的 (填序号)制Cl2 , 反应中浓盐酸所表现出的性质是 
