1.
定性检测和定量测定是科学学习中经常用到的方法。为分析久置于空气中的氢氧化钠是否变质以及变质的程度,科学兴趣小组设计并进行了如下实验:
【定性检测】为判断氢氧化钠是否变质,兴趣小组先按以下流程进行实验:

(1)
以上三个实验中不能达到实验目的的是试管(填试管序号)中的实验。
(2)
通过上述实验现象,小组同学已确定该氢氧化钠固体已经变质,为进一步判断是部分变质还是全部变质,他们又在上述实验基础上选择其中一支试管继续实验,从而得出该氢氧化钠固体部分变质的结论。请简述他们的实验方法和现象:。
(3)
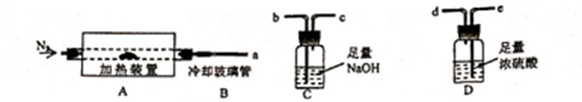
【定量测定】为了测定20g该氢氧化钠样品中碳酸钠的质量分数,兴趣小组设计了如图实验装置进行实验(碱石灰可以吸收水和二氧化碳):
(4)
完全反应后通入N2的目的是。

【实验步骤和数据】
①组装装置,检查气密性;②加入药品,称量C处装置质量为100g,再向A处装置中滴入足量稀硫酸;③完全反应后通入N2;④称量C处装置质量为104.4g。
【实验分析】
利用实验数据可得该部分变质氢氧化钠样品中碳酸钠的质量分数为。
【考点】
实验方案设计与评价;
根据化学反应方程式的计算;
能力提升
真题演练