1.
 气体是一种优良的消毒剂,常用于自来水的消毒。工业上常将
气体是一种优良的消毒剂,常用于自来水的消毒。工业上常将 制备成
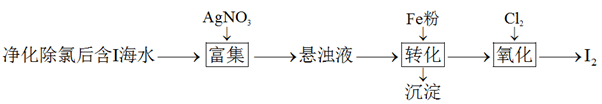
制备成 固体以便运输和贮存,具体流程如图:
固体以便运输和贮存,具体流程如图:

(1)
反应器中发生反应的化学方程式为。
(2)
吸收器中反应时有使带火星的木条复燃的气体产生,则 的作用为(填“氧化剂”或“还原剂”)。
(3)
为了测定获得产品中
的作用为(填“氧化剂”或“还原剂”)。
(3)
为了测定获得产品中 的纯度,进行如下实验:
(4)
以
的纯度,进行如下实验:
(4)
以 和稀盐酸为原料制备
和稀盐酸为原料制备 , 其原理如下:
, 其原理如下: 。当有1mol
。当有1mol 发生上述反应,转移电子的数目为,若盐酸浓度过大,则在上述过程中
发生上述反应,转移电子的数目为,若盐酸浓度过大,则在上述过程中 会发生副反应产生
会发生副反应产生 。写出副反应的离子方程式。
(5)
“有效氯”的定义为:每克含氯消毒剂的氧化能力相当于多少克
。写出副反应的离子方程式。
(5)
“有效氯”的定义为:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。则
的氧化能力。则 的“有效氯”为(保留两位小数)。
的“有效氯”为(保留两位小数)。
①准确称取2.000g上述产品,溶于水配成250.00mL的溶液。
②取25.00mL待测液,加入过量的KI溶液和溶液发生如下反应:
, 杂质不与KI反应。
③以淀粉作指示剂,再加入溶液;恰好完全反应时消耗
溶液的体积为40.00mL。已知:
)。
计算该样品中的纯度。
【考点】
氧化还原反应方程式的配平;
能力提升
真题演练