1.
配制0.9%的NaCl溶液500g,回答下列问题。
(1)计算:需NaCl的质量为g。
(2)称量:托盘天平称量NaCl固体时,应先;(5g以下用游码)。
A 添加砝码
B 调节游码
C 添加NaCl
(3)反思:实际配制的溶液中溶质的质量分数小于0.9%,其原因可能是。
A 氯化钠固体中含有杂质
B 固体倒入烧杯时洒落
C 量筒量取水时仰视读数
D 装瓶时有液体溅出
【考点】
一定溶质质量分数的溶液的配制;
基础巩固
能力提升
变式训练
拓展培优
真题演练

 )。
)。










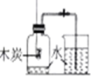 测定空气中氧气的含量
测定空气中氧气的含量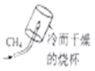 探究甲烷中是否含碳元素
探究甲烷中是否含碳元素 验证质量守恒定律
验证质量守恒定律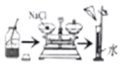 配制一定溶质质量分数的氯化钠溶液
配制一定溶质质量分数的氯化钠溶液