1.
锡 是现代“五金”之一,广泛应用于合金、半导体工业等。
是现代“五金”之一,广泛应用于合金、半导体工业等。
(1)
 位于元素周期表第5周期第IVA族。基态
位于元素周期表第5周期第IVA族。基态 原子的价电子排布式为,其最外层电子云有种伸展方向。
(2)
原子的价电子排布式为,其最外层电子云有种伸展方向。
(2)
 和
和 是锡的常见氯化物。
是锡的常见氯化物。 分子的VSEPR棋型名称为,
分子的VSEPR棋型名称为, 的
的 键是由锡的轨道与氯的
键是由锡的轨道与氯的 轨道重叠形成
轨道重叠形成 键;
键; 的熔点如下表所示:
的熔点如下表所示:
(3)
白锡和灰锡是单质 的常见同素异形体,二者晶胞如图。白锡具有体心四方结构,灰锡具有立方金刚石结构。
的常见同素异形体,二者晶胞如图。白锡具有体心四方结构,灰锡具有立方金刚石结构。
物质 | ||||
熔点 | 705 | 31 | 144.5 |
其熔点呈现上述变化规律的原因为。

①灰锡中每个原子周围与它最近且距离相等的
原子有个;
原子围成的最小环上有个
原子。
②若白锡和灰锡的晶胞体积分别为和
, 则白锡和灰锡晶体的密度之比是。
【考点】
原子核外电子排布;
晶胞的计算;
原子轨道杂化方式及杂化类型判断;
能力提升
真题演练





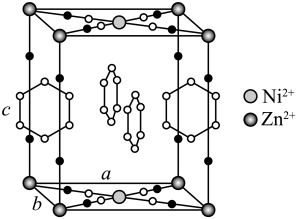
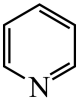 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的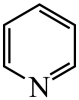 、
、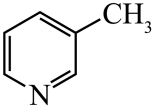 、
、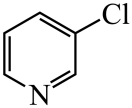 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。




