1.
某中学趣味化学实验小组的同学想通过“被浓
氧化”的实验,验证
的还原性.
实验一:验证的还原性
实验操作 | 预期现象 | 实验现象 |
向盛有2mL | 试管中产生红棕色气体,溶液变为黄色。 | 试管中产生红棕色气体,溶液变为深棕色。 |
(1)红棕色气体是________。(写化学式)
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明________。
(3)根据现象,写出实验一反应的离子方程式:________。
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的或NO与溶液中的
或
反应,而使溶液变为深棕色。
【实验与探究】
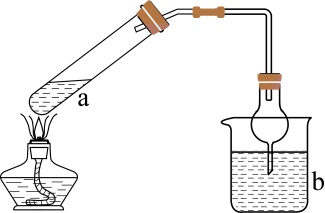
用如图所示装置进行实验(气密性已检验,尾气处理已略去)

ⅰ.关闭c,打开a和b,通入N2 , 一段时间后关闭a;
ⅱ.向甲中加入适量浓 , 一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓 , 一段时间后观察到了与ⅱ相同的实验现象。
(4)装置乙的作用是________(用化学方程式表示)。
(5)实验结论:溶液的深棕色可能是因为 。
| A. | B. |
| C. | D. |
【反思与改进】
实验三:验证的还原性
(6)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有浓硝酸的试管中滴入几滴________,振荡。
(7)可用于
氧化的催化剂。设计从
出发经过3步反应制备
的路线________。
【考点】
化学实验方案的评价;
能力提升
变式训练
拓展培优
真题演练







 C.
C.