1.
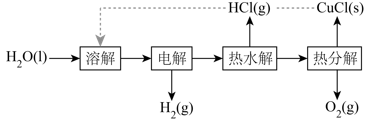
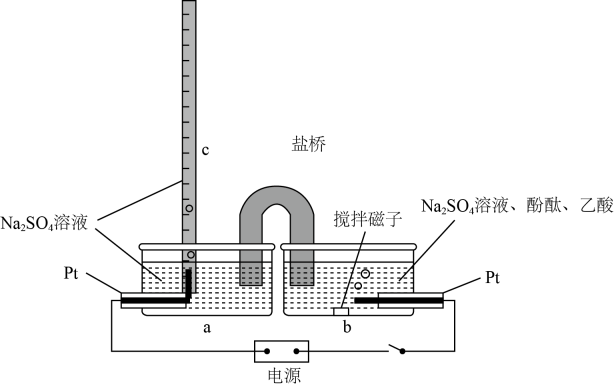
氮氧化物的排放对环境造成很大的污染,研究氮氧化物的转化机理对我们制定保护环境的策略有着重大意义。某科研团队在进行低温下消除氮氧化物的机理研究时,发现NO在转化过程中存在以下核心历程:
①
②
③
(1)
当反应温度为 时,反应最终产物中
时,反应最终产物中 , 若使最终反应产物中
, 若使最终反应产物中 , 则温度T应该
, 则温度T应该 。(填“大于”或“小于”)
(2)
工业上对于电厂烟气中的氨氧化物进行脱硝处理时,通常采用以下反应原理:
。(填“大于”或“小于”)
(2)
工业上对于电厂烟气中的氨氧化物进行脱硝处理时,通常采用以下反应原理: ;
; , 当温度为373℃,压强为
, 当温度为373℃,压强为 情况下,在1L密闭的容器中,通入
情况下,在1L密闭的容器中,通入 、
、 、
、 达到平衡后测定
达到平衡后测定 转化率为60%,体系中
转化率为60%,体系中 , 此时容器中气体总压=
, 此时容器中气体总压= (保留3位有效数字),此时
(保留3位有效数字),此时 转化率为。
(3)
转化率为。
(3)
 条件下,不同温度,在密闭容器中发生反应
条件下,不同温度,在密闭容器中发生反应 , 随着投料比不同,NO平衡转化率变化图像如图所示,图中
, 随着投料比不同,NO平衡转化率变化图像如图所示,图中
 (填“>”,“<”或“=”),NO转化率降低的原因可能是。
(4)
科学家想利用甲烷和氨氧化物设计一款电池,既能提高能源利用率,又能摆脱氮氧化物的污染,反应原理:
(填“>”,“<”或“=”),NO转化率降低的原因可能是。
(4)
科学家想利用甲烷和氨氧化物设计一款电池,既能提高能源利用率,又能摆脱氮氧化物的污染,反应原理: , 酸性介质下,该电池正极的电极反应式为。
(5)
已知基元反应
, 酸性介质下,该电池正极的电极反应式为。
(5)
已知基元反应 的速率方程可表示为:
的速率方程可表示为: (k为速率常数,下同)。碰撞理论研究发现,大多数化学反应并不是经过简单的碰撞就能完成,往往需经过多个反应步骤才反应过程能实现。用
(k为速率常数,下同)。碰撞理论研究发现,大多数化学反应并不是经过简单的碰撞就能完成,往往需经过多个反应步骤才反应过程能实现。用 氧化
氧化 生成
生成 的反应
的反应 实际上经过两步基元反应完成的:
实际上经过两步基元反应完成的:

(快)
(慢)
已知快反应近似平衡态。若在温度为T℃下, ,
。写出T℃下
反应的速率方程:v=(用含
、
、
、a、b的代数式表示)
【考点】
电极反应和电池反应方程式;
能力提升
真题演练