1.
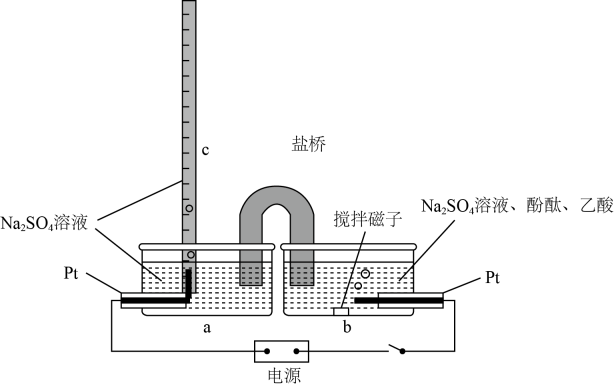
一种简单的原电池装置如图所示。据图回答下列问题。

(1)
锌是该电池的(填“正”或“负”)极。Cu片上发生的电极反应为。能证明化学能转化为电能的实验现象为。
(2)
理论上讲,任何自发的氧化还原反应都可以设计成原电池。请你利用反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池,并回答下列问题:
(3)
下列反应通过原电池装置,不能实现把化学能直接转化为电能的是(填序号)。
①该电池的正极材料是,负极材料是,电解质溶液是溶液。
②在外电路中,电流方向是从极到极。(填“正”或“负”);
③负极电极反应式是;
④若有1mol的Ag析出,转移电子的数目为。
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O
【考点】
电极反应和电池反应方程式;
原电池工作原理及应用;
能力提升
真题演练