1.
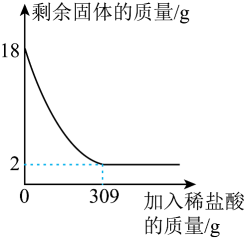
我校在开展中考实验操作后,实验人员用实验室备有的37kg熟石灰对废酸进行中处理,经检测废酸中溶质HCl的质量分数为36.5%。试计算能处理废酸的质量是多少?
【考点】
酸的化学性质;
能力提升
变式训练
拓展培优
真题演练