1.
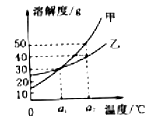
碳酸钠和氯化钠的溶解度曲线如图所示,下列说法错误的是

A.
 点表示
点表示 时,碳酸钠和氯化钠的溶解度相等
B.
碳酸钠的溶解度随温度升高而增大
C.
时,碳酸钠和氯化钠的溶解度相等
B.
碳酸钠的溶解度随温度升高而增大
C.
 时,将
时,将 氯化钠放入
氯化钠放入 水中,充分溶解后得到
水中,充分溶解后得到 溶液
D.
溶液
D.
 时,使接近饱和的碳酸钠溶液变为饱和溶液的最佳途径是加入碳酸钠
时,使接近饱和的碳酸钠溶液变为饱和溶液的最佳途径是加入碳酸钠
【考点】
饱和溶液和不饱和溶液相互转变的方法;
固体溶解度曲线及其作用;
基础巩固
能力提升
变式训练
拓展培优
真题演练