1.
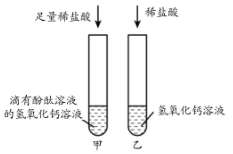
某同学将稀盐酸逐滴加入到氢氧化钡溶液中(如图甲),无明显现象。为确定反应后溶液中溶质组成,他进行以下实验探究:

【建立猜想】猜想①:氢氧化钡过量;猜想②:盐酸过量;猜想③:两者恰好完全反应。
【实验设计】
方案一:取少量反应后溶液于试管1中,滴入少量无色酚酞,溶液不变色,得出猜想①不成立。
方案二:用表中步骤进行探究,得出猜想②成立:
步骤 | 实验操作 | 实验现象 |
Ⅰ | 重新取样,滴加少量紫色石蕊试剂 | 变红 |
Ⅱ | 继续滴加过量的Na2CO3的溶液 | 先产生气泡,后产生白色沉淀,溶液由红色变蓝色 |
(1)
如图乙描述的是氢氧化钡与盐酸反应的微观过程,请从微观角度分析反应的实质是。
(2)
根据实验结果分析可知图甲中反应后溶液中溶质组成是。
(3)
他的同学认为方案二中步骤Ⅱ多余,你认为他的同学的理由是:。
(4)
【拓展探究】
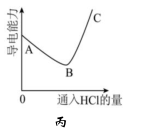
相同条件下,离子浓度越大,电导率越大。他将某Ba(OH)2溶液平均分成两份置于两个烧杯中并插入电导率传感器(如丙图1),往其中一份滴加稀硫酸,往另一份滴加盐酸溶液,测得溶液的电导率变化(如丙图2)所示。结合材料信息和所学知识分析:曲线(选填“甲”或“乙”)对应氢氧化钡与硫酸反应。
【考点】
酸与碱的反应及用途;
能力提升
真题演练