1.
等质量的甲、乙、丙三种金属分别与三份等质量且足量的稀硫酸充分反应(反应后甲、乙、丙三种金属元素均显+2价),生成氢气的质量与反应时间的变化关系如图所示。下列说法正确的是( )

A.
反应消耗硫酸的质量相同
B.
化学反应速率:甲>乙>丙
C.
所得溶液的质量:甲<乙<丙
D.
相对原子质量:甲>乙>丙
【考点】
金属活动性顺序及其应用;
根据化学反应方程式的计算;






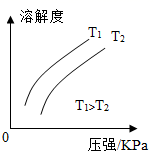 CH4的溶解度与温度、压强的关系
CH4的溶解度与温度、压强的关系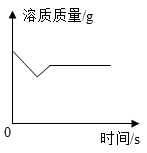 向Ca(OH)2饱和溶液中加少量CaO
向Ca(OH)2饱和溶液中加少量CaO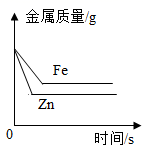 在等质量、等质量分数的两份稀硫酸中,分别加入过量的铁粉、锌粉(铁粉与锌粉质量相等)
在等质量、等质量分数的两份稀硫酸中,分别加入过量的铁粉、锌粉(铁粉与锌粉质量相等)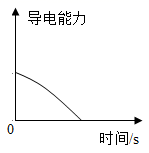 向稀硫酸中,逐滴加入与稀硫酸等质量、等质量分数的氢氧化钡溶液,测溶液的导电能力(离子浓度越大,溶液导电能力越强)
向稀硫酸中,逐滴加入与稀硫酸等质量、等质量分数的氢氧化钡溶液,测溶液的导电能力(离子浓度越大,溶液导电能力越强)