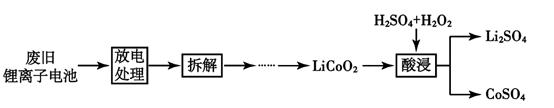
1.
研究氮的氧化物(如:NO、 、
、 )和氮的氢化物都有广泛的用途,如:
)和氮的氢化物都有广泛的用途,如: 和
和 可作为运载火箭的推进剂。
可作为运载火箭的推进剂。
(1)
已知:
 。现将2mol
。现将2mol  放入1L恒容密闭容器中,平衡体系中
放入1L恒容密闭容器中,平衡体系中
 体积分数(
体积分数( )随温度的变化如图所示。
(2)
NO氧化为
)随温度的变化如图所示。
(2)
NO氧化为 的反应为:
的反应为: , 该反应分如下两步进行:
(3)
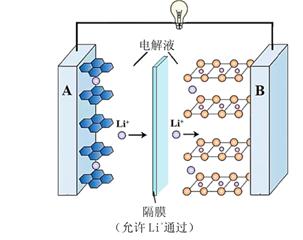
肼除了可作火箭的推进剂外,还可用于新型环保电池中,电池工作原理如图所示。
, 该反应分如下两步进行:
(3)
肼除了可作火箭的推进剂外,还可用于新型环保电池中,电池工作原理如图所示。

①d点v(正)v(逆)(填“>”“=”“<”)。
②a、b、c三点中平衡常数、
、
由小到大是。
③在时,
的平衡转化率为;若平衡时的总压为100kPa,则该反应平衡常数
(保留到小数点后1位)。
Ⅰ.
(较快)
Ⅱ.
(较慢)
在恒容的密闭容器中充入一定量的NO和 , 保持其它条件不变,控制反应温度分别为
和
, c(NO)随t(时间)的变化如图所示。

在反应时间相同时,条件下转化的NO量(填“大于”“等于”“小于”)
条件下转化的NO量,其本质原因是(结合反应Ⅰ和Ⅱ的反应热进行分析)。

①向移动(填“电极甲”或“电极乙”)。
②该电池的负极反应式为。
【考点】
电极反应和电池反应方程式;
化学反应速率;
化学反应速率与化学平衡的综合应用;
化学平衡的计算;
原电池工作原理及应用;
能力提升