1.
X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和等于49.它们的化合物在常温下有如图所示的转化关系:
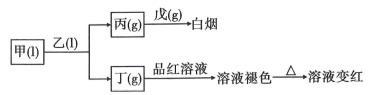
已知:乙、戊分子都含有10个电子,且两种分子中心原子的杂化方式均为杂化,乙中共价键的键角小于戊中共价键的键角。丙易溶于水,0.1mol/L丙的水溶液中,
。甲为三种元素组成的化合物,其他化合物均为两种元素组成的化合物。试回答下列问题:
(1)
Q元素原子的简化电子排布式为。
(2)
甲、乙、丙、丁、戊五种分子中,中心原子杂化方式为 的是(填分子的化学式);乙中共价键的键角小于戊中共价键的键角的原因是。
(3)
戊分子为分子(填“极性”或“非极性”),甲分子的VSEPR模型为。
(4)
写出甲与乙反应的化学方程式:。
(5)
下列说法正确的是____(填序号)。
A.
简单阴离子半径:W>Q
B.
常温下,0.1
的是(填分子的化学式);乙中共价键的键角小于戊中共价键的键角的原因是。
(3)
戊分子为分子(填“极性”或“非极性”),甲分子的VSEPR模型为。
(4)
写出甲与乙反应的化学方程式:。
(5)
下列说法正确的是____(填序号)。
A.
简单阴离子半径:W>Q
B.
常温下,0.1 简单氢化物水溶液的pH:Q>W>Z>Y
C.
最高价氧化物对应水化物的酸性:Q>W
D.
化合物
简单氢化物水溶液的pH:Q>W>Z>Y
C.
最高价氧化物对应水化物的酸性:Q>W
D.
化合物 中含极性键、非极性键和离子键
E.
甲与乙的化学反应中,甲作氧化剂
中含极性键、非极性键和离子键
E.
甲与乙的化学反应中,甲作氧化剂
【考点】
原子核外电子排布;
键能、键长、键角及其应用;
无机物的推断;
元素周期表中原子结构与元素性质的递变规律;
元素周期律和元素周期表的综合应用;
 ,该同学所画的轨道表示式违背了。
,该同学所画的轨道表示式违背了。