1.
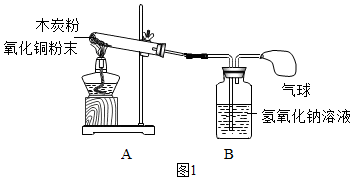
某化学兴趣小组的同学用如图所示装置进行氧化铜与炭粉的反应实验,并对生成气体的成分进行探究。

【查阅资料】NaOH溶液能吸收CO2。
(1)
根据质量守恒定律,对生成气体的成分作出如下猜想:①只有二氧化碳;②只有一氧化碳;③。写出猜想①所发生反应的化学方程式:。
(2)
实验开始时,先打开弹簧夹K,缓缓通入氮气一段时间,然后关闭弹簧夹K,通入氮气的目的是。
(3)
装置A中可观察到的实验现象是;装置B中可观察到澄清石灰水变浑浊,发生反应的化学方程式为;装置C的作用是。
(4)
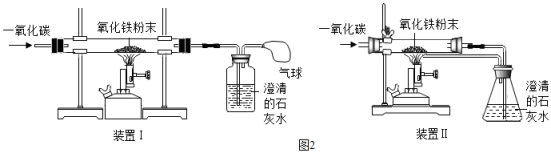
小组同学观察到装置E中有明显的现象发生,则装置D中发生反应的化学方程式为,综合实验现象可知猜想成立。
(5)
小组分析讨论后认为:CO可能是反应生成的CO2和过量木炭在高温下反应生成的,写出该反应的化学方程式:。
(6)
当装置B中不再有气泡冒出时,反应停止,待装置A中玻璃管冷却后倒出固体残留物,其中一定含有铜,可能含有。
(7)
该实验装置还存在明显的不足之处:,你的改进建议是。
【考点】
碳、一氧化碳、氢气还原氧化铜实验;
能力提升
真题演练


 图Ⅱ
图Ⅱ