1.
盐的水解及沉淀的溶解平衡是中学化学研究的重点之一、回答下列问题:
(1)
已知常温下甲酸( )的电离常数
)的电离常数 。
(2)
某酸性工业废水中含有一定量的硫酸铜,其物质的量的浓度为
。
(2)
某酸性工业废水中含有一定量的硫酸铜,其物质的量的浓度为 , 向该溶液中加入氢氧化钠稀溶液除去
, 向该溶液中加入氢氧化钠稀溶液除去 (
( 、
、 、
、 )
(3)
)
(3)
 时,向
时,向 溶液中滴加
溶液中滴加 溶液(一种酸,酸性强弱未知)时,溶液中由水电离的
溶液(一种酸,酸性强弱未知)时,溶液中由水电离的 浓度随加入的
浓度随加入的 体积的变化如图所示:
体积的变化如图所示:
①写出水解反应的离子方程式:,往其溶液中加入下列物质,能促进
水解的是 (填字母)。
A. B.
C.
D.
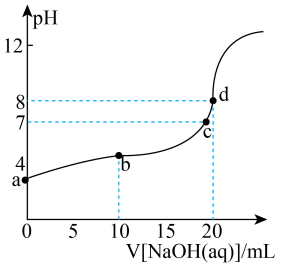
②常温下,向溶液中滴入
的
溶液,溶液的
变化曲线如图所示,d点溶液中
(保留两位有效数字);b点溶液中:
(填“>”“<”或“=”)
。
①常温下要使降低为
, 溶液的
应调至。
②向硫酸铜溶液中通入
气体,该反应的离子方程式为,当溶液中的
时,
。

①若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会(填“增大”“不变”或“减小”)。
②若c点溶液中溶质的总物质的量为 , 向c点溶液中加入
的
, 此时溶液满足的元素质量守恒式为。
【考点】
弱电解质在水溶液中的电离平衡;
水的电离;
盐类水解的原理;
电离平衡常数;
能力提升


