1.
自然界中含硫物质不断发生转化和转移,形成了硫元素的循环。利用这些转化可以制备重要的化工产品,过程中产生的 等会污染环境,需要加以治理。
等会污染环境,需要加以治理。
(1)
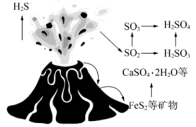
火山喷发是硫元素在自然界中转化的一种途径,反应过程如图所示。
(2)
工业上利用 的转化制备硫酸,其模拟实验的部分装置如图所示。
(3)
的转化制备硫酸,其模拟实验的部分装置如图所示。
(3)
 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 脱硫和
脱硫和 再生的反应机理如图所示。
(4)
再生的反应机理如图所示。
(4)
 的“再生”是在
的“再生”是在 时,用一定浓度的
时,用一定浓度的 与
与 反应实现(如上图所示)。温度略低于
反应实现(如上图所示)。温度略低于 时,“再生”所得固体质量增加,原因是。
时,“再生”所得固体质量增加,原因是。
的结构式为。
与
和
溶液反应转化为
和
, 理论上转移电子的物质的量为
。
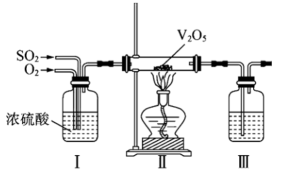
①装置I的作用是(写出两点)。
②装置III用于吸收制备硫酸,适宜的吸收剂是(填字母)。
A.溶液 B.水 C.
浓硫酸
③装置II中待反应进行后撤走酒精灯,无需持续加热,原因是。若用、水在催化剂存在时吸收尾气中的
, 吸收完成后,随着氧化的进行,溶液的
将(填“增大”“减小”或“不变”)。

写出“脱硫”时发生反应的化学方程式。
【考点】
含硫物质的性质及综合应用;
化学实验方案的评价;
结构式;
氧化还原反应的电子转移数目计算;
能力提升



