1.
( 某兴趣小组利用废镍材料(含有金属 Ni 及少量 Fe、 Ag) 探究相关物质的性质并回收镍,设计流程如图所示(部分产物略去)

查阅资料: a.H2O2 溶液可将 Fe2+转化为 Fe3+。
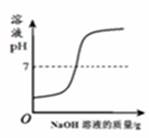
b.Fe3+、 Ni2+转化为对应的氢氧化物沉淀时, 溶液 pH 有如图关系:

(1)
步骤Ⅰ的操作为。
(2)
滤渣①的成分为。
(3)
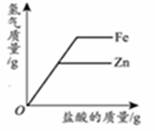
单质 Fe 参与反应的化学方程式为 (任写一个)。
(4)
滤液②中有 Ni2+、 无 Fe3+, 则滤液②pH 可能为____ (填序号)。
A.
pH =1
B.
pH =2
C.
pH =6
D.
pH =10
(5)
Ni、 Fe、 Ag 三种金属的活动性由强到弱的顺序为。
【考点】
金属的化学性质;
金属活动性顺序及其应用;
能力提升
真题演练