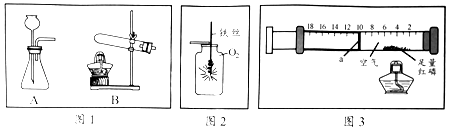
1.
氧气是维持人类生命的重要气体。
(1)
(2)
用C装置来制取氧气,分液漏斗中的药品可为。
(3)
用B装置制取氧气时需要使用催化剂。下列关于催化剂说法正确的是____(填字母)。
A.
该反应不加催化剂就没有氧气生成
B.
在化学反应前后催化剂的化学性质没有改变
C.
加入催化剂不但可以加快反应速度,还可以增加生成氧气的质量
(4)
实验二:家用制氧机可以获得“富氧空气”(氧气含量高于普通空气)
(5)
本次实验测得“富氧空气”中氧气的体积分数为。
(6)
实验三:研究“富氧空气”的应用
实验一:实验室常用如下装置制取氧气。
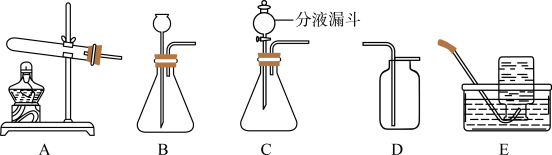
用图3装置测定家用制氧机获得的“富氧空气”中氧气的含量(集气瓶中“富氧空气”体积为100mL,底部残留少量水,燃烧匙内有足量红磷),操作如下:
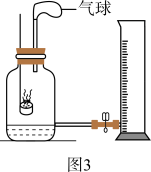
①往量筒内加入适量水,读出量筒内水的体积为100mL;
②点燃红磷,充分反应并冷却至室温;
③打开止水夹,待右侧量筒内液面不再变化时,调节两边液面在同一水平面上,读出量筒内水的体积为18mL。
检查装置气密性:关闭弹簧夹,两手紧握集气瓶。过一会儿,若观察到,证明装置不漏气。
通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如图4。
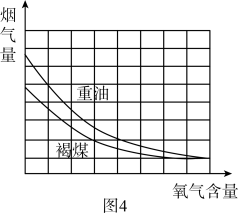
结合图4,简述减少燃料燃烧尾气污染的措施:。
【考点】
测定空气中的氧气含量;
氧气的实验室制法;
催化剂的特点与催化作用;
能力提升
真题演练