1.
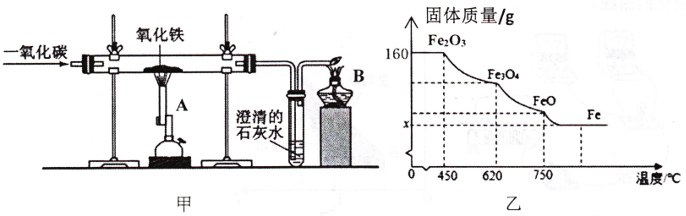
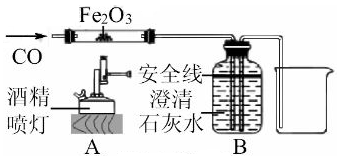
工业上用一氧化碳在高温下还原氧化铁来冶炼铁,某炼铁厂购进1000t含氧化铁质量分数为80%的某种矿石。请计算:
(1)
1000t矿石中含氧化铁的质量。
(2)
杂质不参加反应,理论上可以炼出纯铁的质量是多少?
【考点】
还原反应与金属的冶炼;
能力提升
真题演练