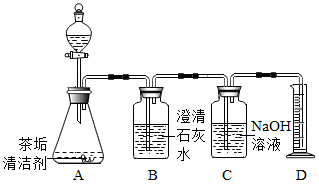
1.
某学习小组的同学以“探究碱石灰成分”为主题开展项目式学习。
(1)
 、 和少量水。
(2)
任务二:探究实验室久置的“碱石灰”样品的成分
、 和少量水。
(2)
任务二:探究实验室久置的“碱石灰”样品的成分
【作出猜想】样品中的成分可能有下列几种: 猜想 :
: 、
、 猜想
猜想 :
: 、
、 、
、 猜想
猜想 :
: 、
、 、
、 猜想
猜想 :
: 、
、
【实验探究】该小组同学设计并进行了如下实验 已知
已知 溶液呈中性
溶液呈中性
(3)
【反思评价】 步骤 的方案不严密,理由是 。改进实验方案:取
的方案不严密,理由是 。改进实验方案:取 “碱石灰”样品于烧杯中, ,则猜想
“碱石灰”样品于烧杯中, ,则猜想 不正确。
(4)
试剂
不正确。
(4)
试剂 可选用 ____
可选用 ____  填字母序号
填字母序号 。
A.
氯化铁溶液
B.
稀盐酸
C.
碳酸钠溶液
D.
二氧化碳
。
A.
氯化铁溶液
B.
稀盐酸
C.
碳酸钠溶液
D.
二氧化碳
任务一:查阅资料认识碱石灰
Ⅰ制碱石灰的流程:

Ⅱ的分解温度是
;
受热不分解。
【作出猜想】样品中的成分可能有下列几种: 猜想
【实验探究】该小组同学设计并进行了如下实验
实验步骤 | 现象 | 结论 |
步骤 加入 | 烧杯底部有白色固体 | 猜想 |
步骤 加入 | 无明显现象 | 猜想 |
步骤 滴 | 溶液变红 | 猜想 |
步骤 加入过量 |
|
【考点】
碱的化学性质;
实验探究物质的组成成分以及含量;
能力提升
真题演练