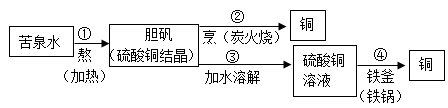
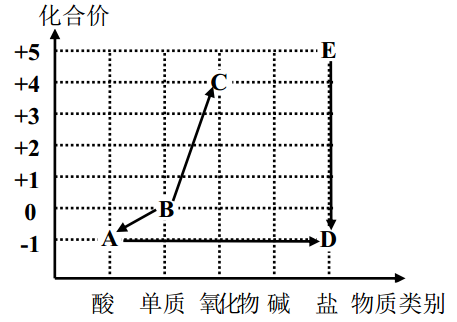
1.
小柯认为实验室可用氢氧化钠溶液吸收多余的二氧化碳,从而实现实验室二氧化碳的“零排放“。小柯同学查阅资料发现,氢氧化钠与二氧化碳反应除了生成碳酸钠外,还有可能生成碳酸氢钠。为此,他就氢氧化钠和二氧化碳反应产物的问题展开探究。
查阅资料:
| 碳酸钠和碳酸氢钠的性质 | ||
| 碳酸钠 | 碳酸氢钠 | |
| 化学式 | Na2CO3 | NaHCO3 |
| 酸碱度 | 饱和溶液的pH约为11.6 | 饱和溶液的pH越为8.3 |
提出方案:可以通过检验反应后的溶液的酸碱度来确定产物。
设计实验:如图甲,利用数字化传感器对吸收二氧化碳后的溶液pH进行实时测定,并通过电脑软件获得实时所与时间曲线如图乙。

请回答下列问题。
(1)
锥形瓶中通过纯碱与稀硫酸反应制取二氧化碳,其化学方程式为 。
(2)
实验中,用磁力搅拌器搅拌的目的是 。
(3)
根据图乙,你觉得能否得出二氧化碳和氢氧化钠反应既能产生碳酸钠,也能产生碳酸氢钠的结论。请发表你的观点并说明理由 。
【考点】
复分解反应及其应用;
能力提升
真题演练