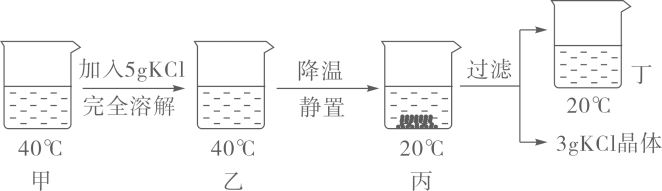
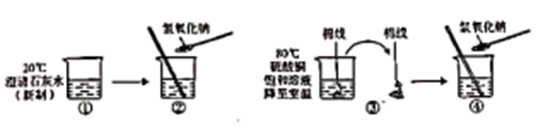
1.
下表是氯化钠和硝酸钾在不同温度下的溶解度。
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度 (g/100g水) | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
(1)
40℃时,比较溶解度大小:KNO3NaCl(填“>”“<”或“=”)。
(2)
20℃时,在100 g水中投入30 g NaCl,为使其快速溶解,可使用的方法是,待充分溶解后,所得是(填“不饱和”或“饱和”)溶液,其质量为g。
(3)
20℃时,在盛有100 g水的A、B两烧杯中分别加入X g的KNO3和NaCl,溶解情况如图所示。

I.A烧杯中加入的物质是(填“KNO3”或“NaCl”),形成的溶液中溶质与溶剂的质量比为。若降温到0℃,烧杯中形成的晶体质量最多为g。
II.实验结束,为了从B烧杯的溶液中回收尽可能多的溶质,可采用的方法是。
【考点】
饱和溶液和不饱和溶液;
固体溶解度的概念;