1.
发生复分解反应的条件是生成沉淀、气体或弱电解质(如水等),利用这一规律,我们可以通过控制条件,使原来“不能进行”的反应真实发生。
(1)
当实验室中盐酸过期无法使用,可通过复分解反应制取少量HCl:NaCl+H2SO4 NaHSO4+HCl↑这是利用了HCl的性。
(2)
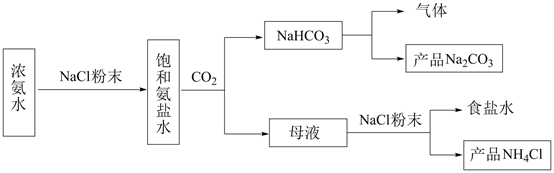
侯氏制碱法的反应原理为:NaCl+H2O+NH3=NaHCO3↓+NH4Cl。某同学在学习了物质分类和转化之后,对该反应原理进行了如下解读:CO2属于,NH3•H2O属于碱,它们反应可生成了一种酸式盐,其化学式为,在一定温度下,该体系中各物质的溶解度如表所示,其中溶解度最小的溶质(即)会析出,也即生成了沉淀反应得以发生。侯氏制碱法的反应原理是否属于离子反应,若是则写出相应的离子方程式。若否请在横线上写“否”。
NaHSO4+HCl↑这是利用了HCl的性。
(2)
侯氏制碱法的反应原理为:NaCl+H2O+NH3=NaHCO3↓+NH4Cl。某同学在学习了物质分类和转化之后,对该反应原理进行了如下解读:CO2属于,NH3•H2O属于碱,它们反应可生成了一种酸式盐,其化学式为,在一定温度下,该体系中各物质的溶解度如表所示,其中溶解度最小的溶质(即)会析出,也即生成了沉淀反应得以发生。侯氏制碱法的反应原理是否属于离子反应,若是则写出相应的离子方程式。若否请在横线上写“否”。
(3)
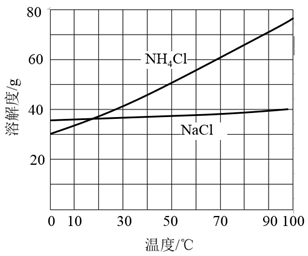
根据各物质的溶解度随温度变化的曲线,欲使KCl+NaNO3=KNO3+NaCl↓发生,应选择的温度可以是(填A或B)。
溶解度/克 | HCO | Cl- | CO |
Na+ | 9.6 | 36.0 | 21.8 |
NH | 21.7 | 372 | 100 |

【考点】
纯碱工业(侯氏制碱法);
能力提升
真题演练



 已知:25℃时,
已知:25℃时, 
 B.
B. 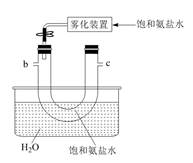 C.
C.  D.
D. 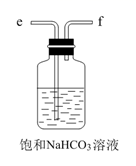 E.
E.