1.
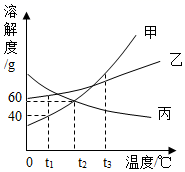
碳酸钠的溶解度曲线如图所示。下列说法正确的是( )

A.
碳酸钠的溶解度随温度升高而增大
B.
将20℃的碳酸钠饱和溶液升温至30℃,溶质质量分数不变
C.
30℃时,将25g碳酸钠加入50g水中,所得溶液质量为75g
D.
40℃时,碳酸钠饱和溶液的溶质质量分数为50%
【考点】
溶解度的影响因素;
固体溶解度曲线及其作用;
溶质的质量分数及相关计算;
基础巩固
能力提升
变式训练
拓展培优
真题演练