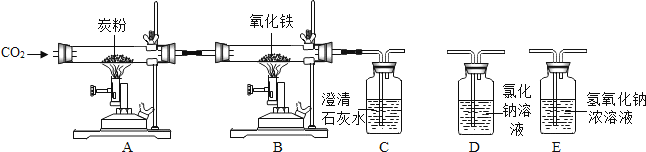
1.
实验探究和证据推理是提升认知的重要手段.化学兴趣小组对“CO还原Fe2O3粉末”的实验进行探究:
(1)
Ⅰ探究CO与Fe2O3的反应产物(夹持仪器已略去)
(2)
【实验现象】反应一段时间后,玻璃管内粉末由色变成黑色,生成的黑色固体均能被玻璃管上方的磁铁吸引.试管Ⅰ中出现白色沉淀(用化学反应方程式表示:.
(3)
【查阅资料】铁粉、FeO、Fe3O4均为黑色固体;铁粉、Fe3O4均能被磁铁吸引.
(4)
【拓展研究】进一步查阅资料,发现CO能溶于铜液[醋酸二氨合铜(Ⅰ)和氨水的混合液].因此可在装置Ⅰ后再连接下图装置Ⅱ,其目的是,装置Ⅰ、Ⅱ的连接顺序:b连接(填“c”或“d”).
(5)
Ⅱ原料气CO的制备

【实验过程】步骤1 在通风橱中,按图Ⅰ连接装置并检验装置的气密性.
步骤2 装入试剂:玻璃管内装入Fe2O3粉末,试管Ⅰ中装入澄清石灰水.
步骤3 从a端通入CO一段时间,待,再点燃酒精灯.
【提出猜想】对磁铁吸引的黑色固体成分有以下三种猜想:
猜测Ⅰ:Fe;猜测Ⅱ:Fe3O4;猜测Ⅲ:Fe和Fe3O4
【实验验证】取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,观察到红色固体中混有黑色颗粒,说明(填“猜想Ⅰ”“猜想Ⅱ”或“猜想Ⅲ”)是正确的.
方法一:加热MgCO3、Zn的混合物可快速制备CO,同时还得到两种金属氧化物:、(填化学式).
方法二:加热草酸晶体(H2C2O4•2H2O)制备CO:
H2C2O4•2H2O CO↑+CO2↑+3H2O
已知:常压下,草酸晶体的熔点为101℃.比较草酸晶体的熔点和分解温度,
分析若选用装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是.
【考点】
金属的化学性质;
一氧化碳还原氧化铁;
实验探究物质的组成成分以及含量;
文字表达式;
能力提升
真题演练